刚刚!CDE新增1个“共性问题解答,涉及电子签章”!
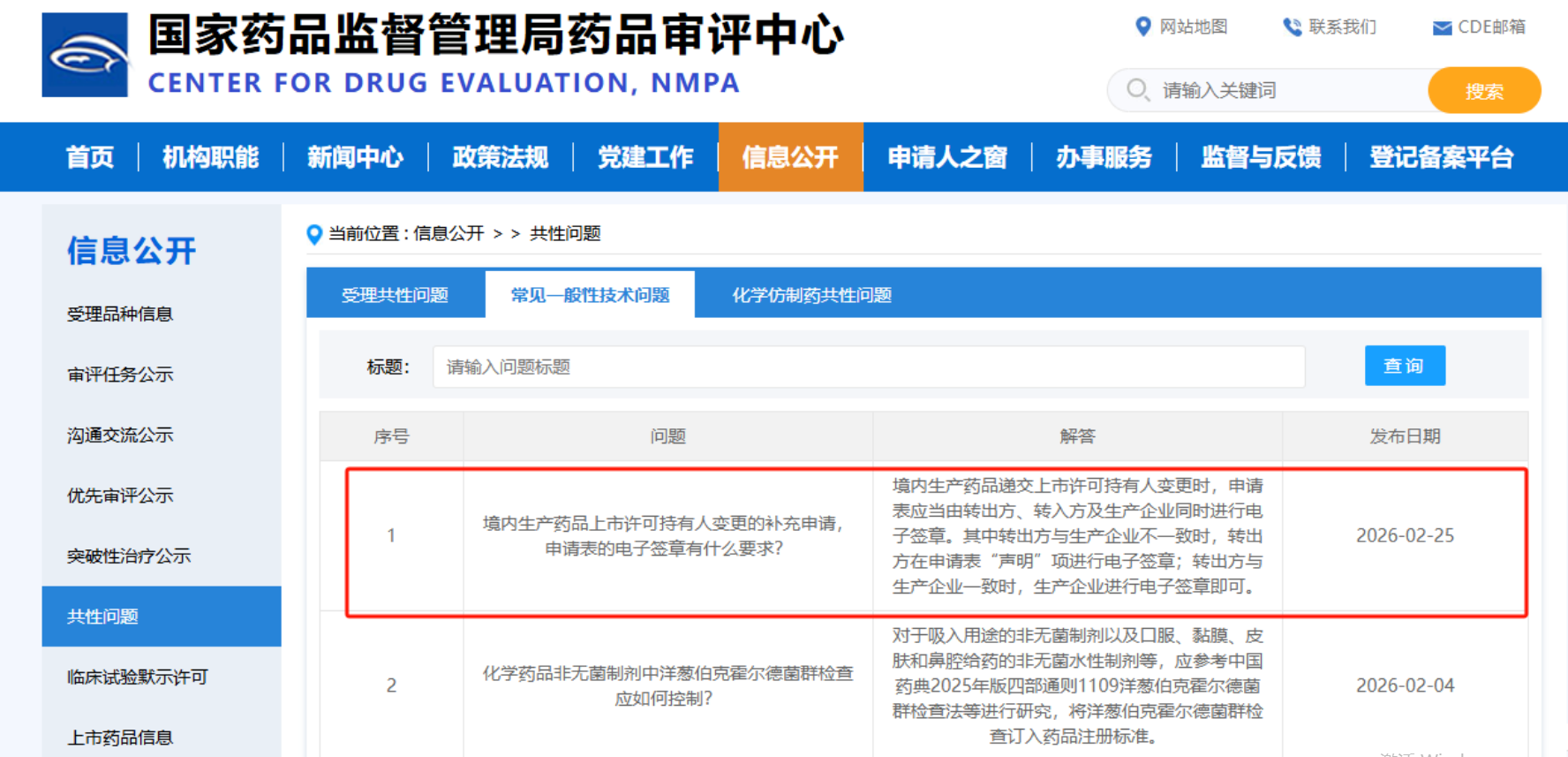
1、境内生产药品上市许可持有人变更的补充申请,申请表的电子签章有什么要求?
答:境内生产药品递交上市许可持有人变更时,申请表应当由转出方、转入方及生产企业同时进行电子签章。其中转出方与生产企业不一致时,转出方在申请表“声明”项进行电子签章;转出方与生产企业一致时,生产企业进行电子签章即可。
相关推荐
涉及5个品种!2020年版《中国药典》第一增补本医学公示内容

湖南省药学会医院制剂研发与真实世界评价应用专委会筹备会议在长沙召开

孙春兰在药品审评中心调研时强调 加快新冠治疗药物研发攻关 为保障人民健康提供有力支撑

中药质量控制技术研讨会在长沙召开,公司领导易跃能博士主讲

喜获硕果|龙年第三个1.1类中药新药获得国家药物临床批件
新发布 | 第一批22个国家中药饮片炮制规范已正式颁布(附全文)
